Натрий

Натрий (Na) - щелочной металл. Натрий, растворяясь в воде образует одну из самых сильных щелочей - едкий натр (или гидроксид натрия). Растворение в воде происходит с бурным выделением тепла и газа (это - водород). Руками металлический натрий брать не желательно - можно обжечься!
Натрий, как другие щелочные металлы, довольно сложно получить в лаборатории, хотя это и можно сделать, например, прокаливая соду с углём:
Na2CO3 + 2С → 3СО + 2Na.
В промышленности натрий получают электролизом расплава смеси хлоридов натрия и кальция (смесь плавится при более низкой температуре, чем чистый хлорид натрия). Интересно, что первым из расплава выделяется не металлический кальций, а более активный - металлический натрий, так как ион Na+ в расплаве легче, чем ион Са2+, принимает электроны. Процесс проводят в стальных электролизёрах при 580 °С. Образующийся жидкий натрий всплывает на поверхность расплава и собирается в специальный приёмник. Ежегодно в мире производится около 200 тыс. тонн натрия, который применяется на атомных электростанциях и в авиадвигателях в качестве теплоносителя, в металлургии — как восстановитель.
Самое извествное химическое соединение натрия - это хлорид натрия или пищевая соль - NaCl. Насколько вредна или полезна эта соль! Когда в рационе слишком много поваренной (пищевой) соли, то в тканях организма задерживается вода, что провоцирует повышенное артериальное давление! А избыток жидкости создаёт дополнительную нагрузку на сердце. Для укрепления сердечной мышцы нужно есть больше продуктов, содержащий калий (K): например капуста и тыква!
Металлический литий

Литий (Li), как и натрий, относится к щелочным металлам. В свободном состоянии литий — серебристый металл белого цвета, мягкий, хотя и твёрже остальных щелочных металлов. Литий, как и натрий, - легкоплавкий металл. Его температура плавления всего tпл=181 °С. Литий настолько лёгок (плотность лития 0,53 г/см3), что не тонет даже в керосине.
Натрий, литий, калий и др. щелочные металлы окрашивают пламя в характерные цвета. Так, наличие ионов лития в веществе придаёт пламени красный цвет, натрия — жёлтый цвет, калия — фиолетовый, а рубидия и цезия — тоже фиолетовый, но более светлого оттенка.
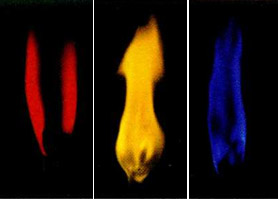
Окрашивание цвета пламени ионами щелочных металлов:
Литий (красный), Натрий (жёлты), Калий (синий)
По сравнению с другими щелочными металлами литий обладает рядом особенностей. Так, при сгорании на воздухе он даёт оксид Li2O, напрямую взаимодействует с азотом, образуя нитрид лития Li3N, и с углеродом, образуя карбид лития Li2C2. Некоторые соли лития (карбонат лития, фторид лития) малорастворимы в воде, а карбонат и гидроксид лития разлагаются при сильном нагреве с образованием оксида лития. Все эти свойства свидетельствуют о том, что химия лития близка к химии магния (Mg).
Титан

Титан (Ti) - серебристый металл белого цвета, тугоплавкий, плавящийся при температуре 1668 °С. Титан обладает невероятной пластичностью — из него можно получить тончайшую фольгу. По прочности титан превосходит чистое железо (при вдвое меньшей плотности), а его коррозионная стойкость исключительно выше — металлический титан можно хранить в морской воде. Благодаря таким замечательным механическим свойствам титан стал незаменимым конструкционным материалом. Титан составляет основу большинства сплавов, используемых в судостроении, авиационной, космической и ядерной технике.
Поразительна химическая стойкость металлического титана. Нередко она более высокая, чем у благородные металлы. На титан, например, не действуют хлорная вода, смесь концентрированных азотной и серной кислот и даже царская водка (золото во всех этих жидкостях растворяется). Объясняется это тем, что уже при обычных условиях на поверхности титана образуется прочная защитная плёнка оксида; под действием же окислителей она становится ещё толще и прочнее.
Исключительно стоек титан и к коррозии. Если в морскую воду погрузить пластинки из чистого алюминия, монеля (медно-никелевого сплава, который используется для чеканки монет), нержавеющей стали и титана толщиной 1 мм, их судьбы окажутся разными. Алюминиевая пластинка уже через несколько дней покроется серыми пятнами (точечная коррозия), а через пять месяцев разрушится. Монелевая — станет тёмно-зелёной из-за взаимодействия меди и никеля с агрессивной морской водой, а примерно год спустя её постигнет судьба алюминиевой. Стальная пластинка продержится года четыре, постепенно покрываясь ржавыми пятнами. Кстати, ракушки и водоросли заметно ускоряют разрушение стали. Титановая же пластинка даже через тысячу лет (!) останется почти невредимой: коррозия проникнет в неё всего на 0,02 мм. В этом отношении титан по стойкости не уступает платине.
Хотя прочная оксидная плёнка надёжно защищает титан от окисления, он довольно легко растворяется в плавиковой и концентрированной соляной кислотах:
Ti + 6HF → H2TiF6 + 2Н2;
2Ti + 6НСl → 2TiCl3 + 3H2
Титан имеет свою «ахиллесову пяту» — он очень «боится» соединений фтора (F). Во фтороводородной (плавиковой) кислоте титан, - обычно стойкий металл, - растворяется чуть ли не так же быстро, как магниевая стружка в соляной кислоте.
 Перейти на английский
Перейти на английский